 El laboratorio BrainStorm Cell Therapeutics ha anunciado que el ensayo clínico de fase 3 con terapia celular NurOwn en 200 pacientes con esclerosis lateral amiotrófica (ELA), ya está totalmente completa la inscripción y el tratamiento está en marcha.
El laboratorio BrainStorm Cell Therapeutics ha anunciado que el ensayo clínico de fase 3 con terapia celular NurOwn en 200 pacientes con esclerosis lateral amiotrófica (ELA), ya está totalmente completa la inscripción y el tratamiento está en marcha.
El ensayo aleatorizado, doble ciego y multicéntrico ( NCT03280056 ) está evaluando la seguridad y la eficacia de tres administraciones de NurOwn en el canal espinal. Los pacientes recibirán inyecciones intratecales NurOwn o placebo cada dos meses.
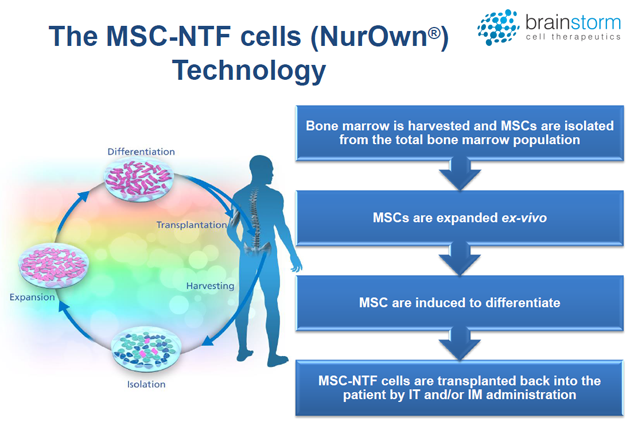
NurOwn es una terapia celular que toma células madre mesenquimales (MSC) de pacientes (MSC autólogas), que pueden generar varios tipos de células. Estas MSC se convierten luego en un tipo de célula, llamadas MSC-NTF, que producen factores neurotróficos (moléculas que promueven el crecimiento y la supervivencia del tejido nervioso). Luego, las células convertidas se devuelven a los pacientes mediante un trasplante, ya sea mediante una inyección en el músculo o en el canal espinal, para promover el crecimiento y la supervivencia del tejido nervioso.
Los objetivos principales del estudio de la seguridad y la eficacia de NurOwn se medirán utilizando el puntaje de la escala de calificación funcional de ALS (ALSFRS-R; un puntaje de habilidades como tragar, hablar, escribir a mano, caminar, etc.) y se compararán con el grupo de placebo.
Un objetivo secundario es evaluar cómo los biomarcadores, como los factores neurotróficos secretados por células, los factores inflamatorios y las citocinas , cambian la sangre y el líquido cefalorraquídeo (el líquido que rodea el cerebro y la médula espinal) después del tratamiento con NurOwn.
«Hasta la fecha, un porcentaje significativo de los 200 pacientes inscritos han recibido tres tratamientos y esperamos que todos los participantes del ensayo completen las visitas y evaluaciones de estudio planificadas para octubre de 2020«, dijo Lebovits.
Este estudio se está llevando a cabo en EE.UU.: en la Universidad de California, Irvine ; Centro Médico Cedars-Sinai ; Centro Médico California Pacific ; Hospital General de Massachusetts ; la Facultad de medicina de la Universidad de Massachusetts ; y la Clínica Mayo .
Si tiene éxito, los resultados de los ensayos se utilizarán para respaldar una solicitud de la FDA para la aprobación de NurOwn como tratamiento de ALS , dijo BrainStorm.
Fuente de la información: Als News Today